非典型溶血性尿毒症症候群(指定難病109)
○ 概要
1.概要
血栓性微小血管症(TMA: thrombotic microangiopathy)は微小血管症性溶血性貧血(MAHA: microangiopathic hemolytic anemia)、消費性血小板減少、微小血管内血小板血栓による臓器機能障害を3主徴とする病態である。TMAは志賀毒素産生性大腸菌感染による溶血性尿毒症症候群(STEC-HUS: Shiga toxin-producing E.coli associated Hemolytic Uremic Syndrome)、ADAMTS13活性著減による血栓性血小板減少性紫斑病(TTP: thrombotic thrombocytopenic purpura)、補体制御異常による非典型溶血性尿毒症症候群(aHUS: atypical HUS)、二次性TMAの4つに分類される。
aHUSは致死率が高く予後が非常に悪い。海外では、毎年100万人あたり成人で2人発症、小児では100万人に7人発症と報告がある。TMAのうち、STEC-HUS、TTP、二次性TMAを鑑別しえた患者で臨床的にaHUSと診断される。臨床的aHUS患者において、さらにaHUSの特異的な検査を行い、既知補体関連の病的遺伝子変異例、抗H因子抗体陽性例がaHUS確定診断例である。医療費助成の対象とすべき疾病の範囲は、2015年の基準による臨床的aHUS診断例、又はaHUS確定診断例のみに対してであり、注意を要する。
2.原因
aHUSはTMAを来す多彩な疾患を含み、そのうちの一部が補体活性化制御因子の遺伝子異常によることが分かってきた。これらの遺伝子異常はaHUS患者の約60%で見つかっている。これまでに先天性の例としCFH、CFI、CD46(MCP)、C3、CFB、THBD、diacylglycerol kinase ε (DGKE)の病的遺伝子変異、後天性の例として抗H因子抗体陽性例がaHUSを起こすと報告されている。ただし、原因の特定できないaHUSもある。補体の遺伝子異常を有していても発症するのは、約30%とされる。
3.症状
aHUSで見られる主な症状としては、血小板数の減少による出血斑(紫斑)などの出血症状や溶血性貧血による全身倦怠感、息切れなどである。また、高度の腎不全によって浮腫、乏尿が認められることもある。時に、発熱や精神神経症状などを認める場合がある。消化器症状(腹痛、下血)を呈することもあり、注意を要する。
4.治療法
現時点での有効な治療法としては、血漿交換や血漿輸注などの血漿療法と、ヒト化抗C5モノクローナル抗体製剤がある。血漿療法は1970年代後半から導入され、aHUS患者の死亡率は50%から25%にまで低下した。aHUS(補体関連HUS)に対しては、ヒト化抗C5モノクローナル抗体が有効であるが、ヒト化抗C5モノクローナル抗体を用いるに当たっては下記の鑑別疾患を参考に、正しく診断することが重要である。
5.予後
aHUSでは、その約半数が血液透析を必要とする高度の腎不全に至ると言われており、致死率が高い理由は腎不全によるものである。1998年から2016年の症例を解析した本邦の報告では、致死率5.4%、末期腎不全に至る割合が15%であった。
○ 要件の判定に必要な事項
1.患者数(令和元年度医療受給者証保持者数)
100人未満
2.発病の機構
不明(遺伝子異常などが示唆されている。)
3.効果的な治療方法
未確立(血漿交換や血漿輸注などの血漿療法、ヒト化抗C5モノクローナル抗体製剤があるが、根本的治療法なし。)
4.長期の療養
必要(約半数が、長期的に透析が必要な高度の腎不全に至る。)
5.診断基準
あり(日本腎臓学会及び小児科学会関与の診断基準あり。)
6.重症度分類
研究班作成の重症度分類を用いて中等症以上を対象とする。
○ 情報提供元
「血液凝固異常症等に関する研究」班
研究代表者 金沢大学大学院 医薬保健学総合研究科保健学専攻 病態検査学講座 教授 森下 英理子
<診断基準>
下記のaHUS確定診断によるDefinite、又は臨床的診断によるDefiniteを対象とする。
診断のカテゴリー
aHUS確定診断によるDefinite:
(1)先天性の補体関連遺伝子異常として、2016年現在で判明しているCFH、CFI、CD46(MCP)、C3、CFB、
THBD、diacylglycerol kinase ε (DGKE)の7遺伝子の病的変異例
(2)後天性のaHUSとして抗H因子抗体陽性例
臨床的診断によるDefinite:
下記の三徴候を認めるTMAのうち、STEC-HUS、TTP、二次性TMA(代謝異常症、感染症、薬剤性、自己免疫性疾患、悪性腫瘍、HELLP症候群、移植後などによるTMA)を除いたものが臨床的aHUSである。
(1)微小血管症性溶血性貧血:ヘモグロビン(Hb) 10g/dL未満 ※
微小血管症性溶血性貧血は、血清LDHの上昇及び血清ハプトグロビンの著減に加え末梢血塗抹標本での破砕赤血球の存在によって診断される。なお、破砕赤血球を検出しない場合もある。
※Hb10g/dL未満を満たさない場合においても、微小血管症性溶血性貧血が存在すれば当該徴候を満たすものとする。
(2)血小板減少:血小板(Plt: platelets) 15万/µL未満
(3)急性腎障害(AKI: acute kidney injury):
小児例では年齢・性別による血清クレアチニン基準値の1.5倍以上
(血清クレアチニンは、日本小児腎臓病学会の基準値を用いる。)
成人例ではAKIの診断基準を用いる。
<鑑別疾患>
1.TMAの診断とTMA類似疾患の鑑別
・溶血性貧血の確認と他疾患の鑑別:LDHの上昇、血液像で破砕赤血球の有無、ハプトグロビン著減の確認、またクームス試験により自己免疫性溶血性貧血を鑑別する。
・急性腎障害を来す他の疾患の鑑別
・播種性血管内凝固症候群(DIC: disseminated intravascular coagulation)の鑑別:PT、APTT、FDP、Dダイマー、フィブリノーゲンなどを測定し、DICの診断基準などを用いて鑑別する。通常、DICは敗血症、悪性腫瘍、血液疾患、外傷などの基礎疾患のもとで発症する。
・悪性貧血の鑑別:悪性貧血はまれにTMAの様な所見を呈することが報告されており、ビタミンB12、葉酸を測定する。一般的に、悪性貧血では網状赤血球は減少していることが多い。
・ヘパリン起因性血小板減少症(HIT: heparin-induced thrombocytopenia)の鑑別
2.STEC-HUSの鑑別
便培養検査、便中の志賀毒素直接検出法、抗lipopolysaccharide(LPS)-IgM 抗体などが、STEC感染を証明するのに有用である。STEC-HUSでは血便を約8割で認め、血液成分が多い重度の血便を伴い、超音波検査では上行結腸壁の著明な肥厚とエコー輝度の上昇が特徴的で、回盲部から肛門側まで肥厚し、重症例では大腸全体に及ぶことも多い。小児では、STEC-HUSがTMA全体の約90%を占めることから、生後6か月以降で、重度の血便を主体とした典型的な消化器症状を伴う症例では、最初に考えるべきである。
3.TTPの鑑別
ADAMTS13活性が10%未満でADAMTS13に対する中和抗体(インヒビター)が陽性であれば、後天性TTPと診断する。ADAMTS13活性が10%未満で同インヒビターが陰性の場合、先天性TTPを疑う。先天性TTPの確定診断には、ADAMTS13遺伝子解析が必要となる。TTP以外のaHUS、HUS、二次性TMAなどでもADAMTS13活性の軽度低下が認められることがあるが、一般的に活性は20%以上である。
4.二次性TMAの鑑別
・コバラミン代謝異常症(特に生後6か月未満で考慮):生後1年以内に、哺乳不良、嘔吐、成長発育不良、活気低下、筋緊張低下、痙攣などを契機に発見される例が多いが、近年、成人例の発症例も報告されている。血漿ホモシスチン、血漿メチルマロン酸、尿中メチルマロン酸などを測定する。
・自己免疫疾患・膠原病:全身性エリテマトーデス、強皮症クリーゼ、抗リン脂質抗体症候群、多発性筋炎/皮膚筋炎、血管炎:これらの疾患はTMAを呈することがあるため、必要に応じて以下の検査を提出する。
抗核抗体、抗リン脂質抗体、抗DNA抗体、抗セントロメア抗体、抗 Scl-70抗体、C3、C4、CH50、IgG、
IgA、IgM、抗好中球細胞質抗体(ANCA: Anti-neutrophil cytoplasmic antibody)など。
・加速型-悪性高血圧:ただし、aHUSでも高血圧を呈することが多いので鑑別には注意が必要である。
・悪性腫瘍:進行性の悪性腫瘍によりTMAを来すことがある。症例報告をまとめたレビューでは、消化器系癌、乳癌、前立腺癌、肺癌などが多く、9割以上で転移を認める進行性の悪性腫瘍であったとの報告がある。
・感染症:肺炎球菌感染症の中でも、特に侵襲性肺炎球菌感染症がTMAを呈することがあり、小児に認められる。侵襲性肺炎球菌感染症とは、重症肺炎、髄膜炎、菌血症、敗血症、膿胸等を生じる重症肺炎球菌感染症と定義される。国立感染症研究所の報告では5歳未満では本邦で年間300例程度の報告がある。TMA発症は乳幼児が主であり、0.6%程度がTMAを発症するとされる。肺炎球菌が産生するニューラミニダーゼによって露出するThomsen—Friedenreich (T)抗原に対する抗T-IgM抗体が血漿中に存在するため、血漿投与により病状が悪化する可能性がある。直接Coombs試験が約90%の症例で陽性を示す。新鮮凍結血漿を用いた血漿交換療法や血漿輸注等の血漿治療や非洗浄血液製剤の投与は行わない。
その他、HIV、インフルエンザAウイルスH1N1亜系、C型肝炎ウイルス、サイトメガロウイルス感染症、
百日咳、水痘、重症溶連菌感染症などがTMAを起こすことが報告されている。ただし、インフルエンザウイルスなどの感染を契機としてaHUSが発症する例もあるので注意が必要である。
・妊娠関連のHELLP症候群、子癇:HELLP症候群(妊娠高血圧症に合併する溶血性貧血、肝障害、血小板減少)、子癇(妊娠中の高血圧症とけいれん)は、分娩により速やかに軽快する。ただし、TTPやaHUSでも妊娠を契機に発症する例が報告されており、特にaHUS患者では分娩後の発症も多いと報告されるがHELLP症候群においての割合は不明であり、今後の検討課題である。
・薬剤性TMA:抗悪性腫瘍薬、抗血小板剤、免疫抑制剤などが原因となり、TMAを発症することがある。
・急性膵炎:急性膵炎の経過中にTMAを呈することがある。
・造血幹細胞・臓器移植後TMA:造血幹細胞移植後のTMAが特によく知られている。ADAMTS13活性は10%未満には著減せず、血漿交換の有効性は低い。腎移植後に発症するTMAは、原疾患がaHUSで腎不全に陥った症例のaHUSの再発、腎移植後に新規で発症したaHUS、臓器移植に伴う移植後TMAが疑われる。aHUS患者に腎移植を行った場合、TMAの再発と移植腎の廃絶率が高いことから、aHUSが疑われる腎不全患者に腎移植を検討する場合は、移植前に遺伝子検査を行うことが推奨される。その他、肝、心、肺、小腸移植後のTMAの発症も報告されている。
自己免疫疾患・膠原病、造血幹細胞移植後、腎移植後などの二次性TMAでも、補体関連遺伝子異常が認められるとする報告や、抗H因子抗体が陽性である例が報告されている。しかし、二次性TMAの原因としてどこまで補体系の活性化異常が関与しているのか、二次性TMAの中で遺伝子変異のある患者の割合に関しては、今後の検討課題である。
<重症度分類>
中等症以上を対象とする。
aHUS 重症度分類
1.微小血管症性溶血性貧血(Hb 10.0 g/dL未満)※
2.血小板減少(Plt 15万/µL未満)
3.急性腎障害(成人はAKI 病期2以上、小児については添付表の年齢・性別ごとの血清クレアチニン中央値の2倍値以上)
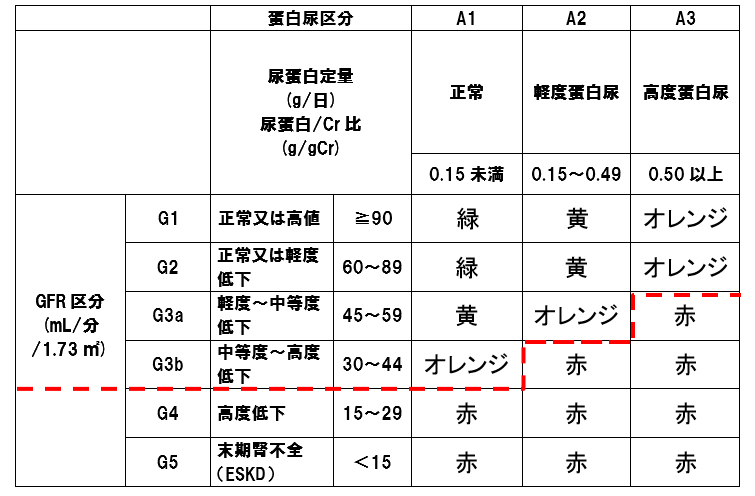
4.慢性腎臓病(小児又は大人のCKD重症度分類ヒートマップが赤の部分の場合)
5.精神神経症状
6.心臓障害(虚血性心疾患、心不全等)
7.呼吸障害
8.虚血性腸炎
9.高血圧緊急症(多くは収縮期血圧180mmHg以上、拡張期血圧は120mmHg以上を示し、その他に高血圧に起因する標的臓器症状を有する。)
10.血漿治療抵抗性
11.再発例
12.血漿治療又は抗補体抗体治療依存性
微小血管症性溶血性貧血は、血清LDHの上昇及び血清ハプトグロビンの著減に加え末梢血塗抹標本での破砕赤血球の存在によって診断される。なお、破砕赤血球を検出しない場合もある。
※Hb10g/dL未満を満たさない場合においても、微小血管症性溶血性貧血が存在すれば当該徴候を満たすものとする。
軽 症 下記以外
中等症 1と2を満たす
重 症 1あるいは2を満たし、3~12のいずれかを満たす
AKI病期(KDIGO 2013)
文献 KDIGO Clinical Practice Guideline for Acute Kidney Injury Kidney International Supplements (2012) 2,1-138
|
|
血清クレアチニン |
尿量 |
|
病期1 |
基礎値の1.5~1.9倍 |
6から12時間で<0.5mL/kg/時 |
|
病期2 |
基礎値の2.0~2.9 倍 |
12時間以上で<0.5mL/kg/時 |
|
病期3 |
基礎値の3倍若しくは血清クレアチニン≥4.0mg/dL の増加、 |
24時間以上で<0.3mL/kg/時 |
基礎値の実測値がない場合は、予測される基礎値で判定。
日本人小児の年齢・性別ごとの血清クレアチニン基準値
|
年齢 |
50%タイル値 |
|
3~5か月 |
0.2 |
|
6~8か月 |
0.22 |
|
9~11か月 |
0.22 |
|
1歳 |
0.23 |
|
2歳 |
0.24 |
|
3歳 |
0.27 |
|
4歳 |
0.3 |
|
5歳 |
0.34 |
|
6歳 |
0.34 |
|
7歳 |
0.37 |
|
8歳 |
0.4 |
|
9歳 |
0.41 |
|
10歳 |
0.41 |
|
11歳 |
0.45 |
|
12歳 男 |
0.53 |
|
12歳 女 |
0.52 |
|
13歳 男 |
0.59 |
|
13歳 女 |
0.53 |
|
14歳 男 |
0.65 |
|
14歳 女 |
0.58 |
|
15歳 男 |
0.68 |
|
15歳 女 |
0.59 |
|
16歳 男 |
0.73 |
|
16歳 女 |
0.59 |
CKD重症度分類ヒートマップ
※診断基準及び重症度分類の適応における留意事項
1.病名診断に用いる臨床症状、検査所見等に関して、診断基準上に特段の規定がない場合には、いずれの時期のものを用いても差し支えない(ただし、当該疾病の経過を示す臨床症状等であって、確認可能なものに限る。)。
2.治療開始後における重症度分類については、適切な医学的管理の下で治療が行われている状態であって、直近6か月間で最も悪い状態を医師が判断することとする。
3.なお、症状の程度が上記の重症度分類等で一定以上に該当しない者であるが、高額な医療を継続することが必要なものについては、医療費助成の対象とする。
- 日本腎臓学会、日本小児科学会 非典型溶血性尿毒症症候群(aHUS)診断基準
- 疾患解説動画
https://www.youtube.com/watch?v=GfOi_b2T6jQ&t=19s
| 研究班名 | 血液凝固異常症等に関する研究班 研究班名簿 研究班ホームページ |
|---|---|
| 情報更新日 | 令和6年4月(名簿更新:令和5年6月) |
(公財)難病医学研究財団
- 補体阻害剤による治療歴のない成人 aHUS 患者を対象としてLNP023 の 1 日 2 回経口投与時の有効性及び安全性を評価する多施設共同,単群,非盲検,臨床試験
- aHUS患者を対象として抗C5抗体薬からiptacopanによる治療に切り替えた場合の有効性及び安全性を評価する多施設共同,単群,非盲検試験
