パーキンソン病(指定難病6)
1.「パーキンソン病」とはどのような病気ですか
振戦(ふるえ)、動作緩慢、筋強剛(筋固縮)、姿勢保持障害(転びやすいこと)を主な運動症状とする病気で、50歳以上で起こることが多い病気です。まれに40歳以下で起こる方もあり、若年性パーキンソン病と呼んでいます。
2.この病気の患者さんはどのくらいいるのですか
10万人に100人~180人くらいです(1000人に1人~1.8人)。65歳以上では100人に約1人(10万人に1000人)で、高齢者では多くなりますので、人口の高齢化に伴い患者さんは増加しています。高齢化やおそらく環境因子、ライフスタイルの変化などに伴い世界的にパーキンソン病が急増する状況は「パーキンソンパンデミック」と呼ばれ、警鐘が鳴らされています。
3. この病気はどのような人に多いのですか
嗜眠性脳炎などの後遺症として起こった記録もありますが、ほとんどの方では特別な原因はありません。神経細胞の中にアルファ-シヌクレインというタンパク質が凝集して溜まることが原因となることが分っていますが、食事や職業、住んでいる地域など、原因となる特別な理由は分っていません。
4.この病気の原因はわかっているのですか
大脳の下にある中脳の黒質ドパミン神経細胞が減少して起こります。ドパミン神経が減ると体が動きにくくなり、ふるえが起こりやすくなります。ドパミン神経細胞が減少する理由はわかっていませんが、現在はドパミン神経細胞の中にアルファ-シヌクレインというタンパク質が凝集して蓄積し、ドパミン神経細胞が減少すると考えられています。このアルファ-シヌクレインが増えないようにすることが、治療薬開発の大きな目標となっています。
5. この病気は遺伝するのですか
遺伝はしませんが、若く発症される方の一部では家族内に同じ病気の方がおられ、病気の原因となる遺伝子が確認されることがあります。
6. この病気ではどのような症状がおきますか。
振戦(ふるえ)、動作緩慢、筋強剛(筋固縮)、姿勢保持障害(ころびやすいこと)が主な運動症状です。ふるえは静止時の振戦で例えば手の場合、椅子に座って膝に置いている時や歩いているときなど力を入れていない時に起こります。動かすとふるえは小さくなります。筋強剛は自分ではあまり感じませんが、他人が手や足、頭部を動かすと感じる抵抗を指しています。動作緩慢は動きが遅くなることで、同時に細かい動作がしにくくなります。最初の一歩が踏み出しにくくなる「すくみ」が起こることもあります。姿勢保持障害はバランスが悪くなり転倒しやすくなることです。姿勢保持障害は病気が始まって数年してから起こります。最初から起こることは無く、病気が始まって2年以内に姿勢保持障害が起こるときには、進行性核上性麻痺などの パーキンソン症候群 の可能性があります。運動症状のほかには、便秘や頻尿、発汗、易疲労性(疲れやすいこと)、嗅覚の低下、 起立性低血圧 (立ちくらみ)、気分が晴れない(うつ)、興味が薄れたり意欲が低下する(アパシー)などの症状も起こることがあり、非運動症状と呼んでいます。
7. この病気にはどのような治療法がありますか
治療の基本は薬物療法です。ドパミン神経細胞が減少するため少なくなったドパミンを補います。ドパミン自体を飲んでも脳へは移行しないため、ドパミン前駆物質のL-ドパ(レボドパ)を服用します。L-ドパは腸から吸収され 血液脳関門 を通って脳内へ移行し、ドパミン神経細胞に取り込まれてドパミンとなります。その後シナプス小胞にとりこまれ、運動調節のために放出されドパミン受容体に作用します。ドパミン受容体刺激薬はドパミン神経細胞を介さずに、直接ドパミン受容体に作用し、少なくなったドパミンを補う作用があります。ドパミン神経以外の作用薬には、アセチルコリン受容体に作用する抗コリン薬、グルタミン酸受容体に作用するアマンタジン、アデノシン受容体に作用するイストラデフィリン、シグマ受容体に作用するゾニサミドがあります。また、L-ドパの作用を強める代謝 酵素阻害薬 があります。L-ドパが腸、肝臓、血管内でドパミンに変わるのを防ぐドパ脱炭酸 酵素 阻害薬(DCI)(カルビドパ、ベンセラジド)、同様にL-ドパが脳に入る前に分解されるのを防ぐカテコール-O-メチル基転移酵素阻害薬(COMT-I)(エンタカポン、オピカポン)、脳内でドパミンが分解されるのを防ぐモノアミン酸化酵素-B(MAO-B)阻害薬(セレギリン、ラサギリン、サフィナミド)があります。いずれもドパミンの作用を強めるように働きます。ドパ脱炭酸酵素阻害薬、カテコール-O-メチル基転移酵素阻害薬はL-ドパとの合剤もあります。
デバイス補助療法(DAT)には手術療法、L-ドパ・カルビドパ配合経腸用液療法とホスレボドパ/ホスカルビドパ配合持続皮下注療法があります。手術療法は脳内に電極を入れて視床下核を刺激する方法が最もよく行われます。視床下核は運動を抑制していると考えられています。ここを刺激して視床下核の機能を制御すると運動の抑制がとれて体が動きやすくなります。薬で治療しても振戦の強い方や、薬の効果が弱まって効いている時間が短くなるウェアリングオフが出現した方で、有効性が期待されます。L-ドパ・カルビドパ配合経腸用液療法では、ゲル状にしたL-ドパを胃ろうから小腸まで挿入したチューブを通してポンプで持続的に投与することで薬の効果を維持します。ホスレボドパ/ホスカルビドパ配合持続皮下注療法では、注射薬のレボドパ前駆薬(プロドラッグ)を24時間持続で皮下注を継続することで運動合併症を治療します。
体を動かすことは体力を高め、パーキンソン病の治療になります。激しい運動ではなく、散歩やストレッチなど、毎日運動を続け体力を高めることは重要です。また、気持ちを明るく保つことも重要です。気分が落ち込むと姿勢も前かがみとなり、動作も遅くなります。私たちが意欲を持って行動する時は脳内でドパミン神経が働いていると考えられています。日常生活の過ごし方も大事な治療ですので、是非工夫してください。
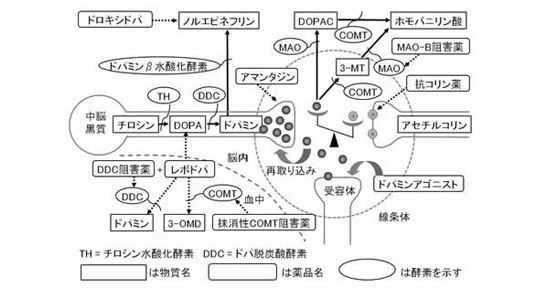
<図の説明>
ドパミンの原料はチロシンです。チロシンはチロシン水酸化酵素(TH)の働きでL-ドパに、L-ドパはドパ脱炭酸酵素(DDC)の働きでドパミンになります。ドパミンは中脳の黒質にあるドパミンを作る細胞で作られ、突起を通り線条体まで運ばれ、ここで突起の先端に貯蔵されます。ドパミンは必要に応じて突起の先端から分泌され、線条体の細胞にあるドパミン受容体に結合して情報を伝えます。仕事を終えたドパミンはドパミンを作る細胞の突起の先端に取り込まれて再利用されるとともに、モノアミン酸化酵素(MAO)あるいはカテコール-O-メチル基転移酵素(COMT)と呼ばれる酵素によって分解されます。線条体ではドパミンのほかにアセチルコリンという 神経伝達物質 があって、両者はバランスをとっています。パーキンソン病ではドパミンが減少するため、相対的にアセチルコリンの機能が過剰になります。これが抗コリン薬を治療に使う理由です。ドパミンはドパミンβ水酸化酵素の働きでノルエピネフリンになります。パーキンソン病が進行すると、ノルエピネフリンも不足し低血圧などの原因になります。
薬物療法
1)L-ドパ(レボドパ)
最も強力なパーキンソン病治療薬です。1970年代のこの薬の登場は、パーキンソン病の治療に画期的な進歩をもたらしました。それまで発症後5年で寝たきりだったのが、10年経っても歩けるようになりました。ところがL-ドパの服薬期間が長くなると、さまざまな問題が起こります。最大の問題は薬効の変動です。L-ドパの血中半減期は短いため、ドパミン神経が変性して脳内に十分なドパミンを貯蔵できなくなると、L-ドパを内服して2~3時間すると効果が切れて動けなくなることがあります。これをウェアリングオフ(wearing-off)現象と呼びます。さらに進行すると神経系の過敏性が生じて、身体が不随意に動いてしまうL-ドパ誘発性の 不随意運動 (ジスキネジア)が出現することもあります。
パーキンソン病の脳内で不足するのはドパミンです。脳内のドパミンを補充すれば元のように動けるようになりますが、ドパミンは血液中から脳内に入りません。そこでドパミンの前駆体でアミノ酸の一種であるL-ドパを薬として服用します。しかし消化管や血液中にはL-ドパをドパミンにするドパ脱炭酸酵素(DDC)が豊富にあるため、L-ドパだけ服薬するとドパ脱炭酸酵素により分解されてしまいます。そこで1980年以降わが国ではL-ドパと末梢性ドパ脱炭酸酵素阻害薬との合剤が一般的に用いられています。なお、L-ドパは血液中のカテコール-O-メチル基転移酵素(COMT)という酵素によっても分解されます。そこでカテコール-O-メチル基転移酵素阻害薬であるエンタカポンやオピカポンを同時に服薬することも行われています。レボドパとドパ脱炭酸酵素阻害薬とカテコール-O-メチル基転移酵素阻害薬の合剤も使われます。
2)ドパミンアゴニスト
L-ドパの副作用を克服するために開発されたのが、作用時間の長いドパミン受容体刺激薬(アゴニスト)です。我が国では現在8種類のドパミンアゴニストが使用可能です。ドパミンアゴニストは長くのみ続けても、薬効の変動( ウェアリングオフ現象 )や ジスキネジア が生じにくいことがわかっています。しかしL-ドパより効くのに時間がかかり、また、吐き気や 幻覚 ・ 妄想 などの副作用に注意が必要です。若年例など運動合併症(ウェアリングオフやジスキネジア)が起きやすいと予想される症例では、L-ドパではなくドパミンアゴニストやモノアミン酸化酵素B阻害薬(MAOB-I)で治療を開始することを検討します。それ以外の症例では、最初からL-ドパで治療開始することで、より確実な効果が期待できます。8種類のドパミンアゴニストはそれぞれ特徴があるので、使い分けが必要です。詳しくは専門の先生と相談してください。また、ペルゴリドやカベルゴリンで心臓弁膜症や肺線維症が起きることがあります。そこで、これらの薬を使用するときは心エコー検査等で定期的に心臓の弁をチェックすることになっています。一方、プラミペキソールやロピニロール、貼付薬のロピニロールやロチゴチン、自己注射薬のアポモルヒネでは、運転中に突然入眠して事故を起こす「突発的睡眠」が起こることがあるため、服薬中は運転しないよう警告が出されています。
3)抗コリン薬
パーキンソン病の治療薬として最初に使われるようになった薬です。トリヘキシフェニジールが良く使われています。なお、高齢者が抗コリン薬をのむと、物忘れや幻覚・妄想など認知機能障害に関連した症状が出ることがあるので、使用の際には注意が必要です。
4)塩酸アマンタジン
塩酸アマンタジンは元来抗ウイルス薬として開発され、A型インフルエンザの治療薬としても使われています。線条体でのドパミン放出を促す働きがあるほか、高用量ではジスキネジアを抑制する効果が知られています。ただし全ての患者さんに有効なわけではなく、また副作用として幻覚や妄想が出やすいので注意が必要です。特に高齢者など腎機能低下のある方では用量を減らす必要があります。
5)ゾニサミド
この薬は、既にてんかんの治療薬として使われていましたが、2009年にパーキンソン病に使うことが認められました。パーキンソン病に使う場合は、1錠がゾニサミド25mgで、50mgまで使います。一方、てんかん予防に使う場合は、1錠がゾニサミド100mgです。間違えないようにしましょう。どうしてパーキンソン症状を改善するのか、その理由は完全には解明されていません。L-ドパとの併用で使う薬で、ウェアリングオフや振戦(ふるえ)に有効です。作用時間が長い薬なので、1日1回の服薬で十分です。
6)アデノシン受容体拮抗薬
日本で開発された薬(イストラデフィリン)で、ウェアリングオフを改善します。ウェアリングオフを軽くする作用がありL-ドパと併用します。ウェアリングオフの改善以外の作用については、まだ充分に解っていません。
7)モノアミン酸化酵素-B(MAO-B)阻害薬
モノアミン酸化酵素-B(MAO-B)阻害薬である塩酸セレギリンやラサギリン、サフィナミドはMAO-Bの活性を低下させてドパミンの分解を抑制します。これによりL-ドパの効果は延長しますが、ジスキネジアが悪化することがあります。モノアミン酸化酵素-B(MAO-B)阻害薬はノルエピネフリンやセロトニンなど他の神経伝達物資の分解も弱く抑制することがあるので、服薬すると意欲が出て気分が明るくなる傾向があります。その一方で、幻覚・妄想や夜間不眠、血圧の変動などに注意が必要です。作用時間は非常に長いので、1日1回(朝)か2回(朝と昼)の服薬で十分です。
8)カテコール-O-メチル転移酵素(COMT)阻害薬
吸収されたL-ドパは血液に入り、血液脳関門を通って脳に入ります。血液の中にはドパ脱炭酸酵素(DDC)やカテコール-O-メチル転移酵素(COMT)という酵素があり、L-ドパを分解します。現在使われているL-ドパ製剤の多くは、L-ドパと末梢性ドパ脱炭酸酵素阻害薬の合剤です。このため、L-ドパはカテコール-O-メチル転移酵素によって分解されます。末梢性カテコール-O-メチル転移酵素阻害薬のエンタカポンやオピカポンはそれを防いでL-ドパが脳内にたくさん入るようにする薬です。エンタカポンの場合は薬効時間が短いので、毎回L-ドパと同時に服薬する必要があります。
9)ドロキシドパ
長期間経過したパーキンソン病で問題になる症状のひとつに、「足のすくみ」があります。これにはもう一つの神経伝達物質であるノルエピネフリンの関与が示唆されています。ノルエピネフリンはβ水酸化酵素によってドパミンから合成されるため、ドパミンが減るとやがて不足します。前駆体であるドロキシドパはそれを補うために使われます。ただし全ての患者さんに有効なわけではありません。このほか意欲低下や立ちくらみを改善する効果が知られています。ドロキシドパは日本で開発された薬で、欧米では立ちくらみの治療薬として承認されています。
パーキンソン病では、一般に複数の薬を組み合わせて治療しています。薬によって、服薬のタイミングが異なりますので、その理由をよく理解して服薬することが大切です。また、パーキンソン病の治療薬以外の薬を併用するときには、飲み合わせに注意することも大切です。服薬する全ての薬を、主治医や薬剤師に確認してもらってください。
手術療法やデバイス補助療法(DAT; Device-Aided Therapy)など
パーキンソン病の手術療法の歴史は長く、定位脳手術が開発されたのは1947年のことです。定位脳手術とは、頭蓋骨に固定したフレームと脳深部の目標点の位置関係を三次元化して、外から見ることのできない脳内の目標点に正確に到達する技術です。頭蓋骨に開けた小さな穴から針を刺すだけなので、手術侵襲は軽くて済みます。1950年代から60年代にかけて、この手術はさかんに行われました。当時はCTスキャンもMRIも無い時代で手術の危険性は高かったのですが、有効な薬が誕生する前だったため、手術を希望する人がたくさんいました。1970年に特効薬のL-ドパが出現すると、手術を受ける人は激減しました。しかし、L-ドパ治療の長期の問題点に対して、1980年代後半から再び定位脳手術が見直されています。定位脳手術には、熱を加えて目標点を凝固する従来の方法(凝固術)のほか、脳深部刺激療法(DBS:deep brain stimulation)があります。DBSは脳深部に電極を留置し、前胸部に植え込んだ刺激装置で高頻度刺激する治療法です。高頻度刺激すると、神経細胞は活動を休み、そこを凝固したのと同じ効果が得られます。我が国では2000年4月から 保険適用 が認められました。DBSは脳を破壊しないので手術合併症が少ないかわり、異物が体内に残るため感染や断線のリスクがあります。
パーキンソン病の定位脳手術は特殊な技術を要するため、限られた病院でのみ実施されています。手術療法も、病気の原因を根本的に治す根治療法ではなく、症状を改善する対症療法です。手術は服薬と比べてリスクを伴いますので、現在の病状や予想される結果を主治医と十分相談してから受けることが大切です。
その他、MRガイド下集束超音波治療(FUS)やL-ドパ・カルビドパ配合経腸用液(LCIG)療法、ホスレボドパ/ホスカルビドパ配合持続皮下注療法などの治療も行われます。
8. この病気はどういう経過をたどるのですか
治療薬が研究開発され、現在のパーキンソン病の平均寿命は全体の平均とほとんど変わらないと考えられています。転倒による骨折や他の病気を併発しないことはパーキンソン病の経過にとても大事です。誤嚥して肺炎を起こしたり便秘して腸閉塞を起こすこともあります。食事は楽しんで、よくかんでゆっくり食べましょう。排便調節に注意を払い週に2回以上は排便があるように体調を保ちましょう。
9. この病気は日常生活でどのような注意が必要ですか
運動、睡眠、食事、薬が基本です。運動は健康維持に必須です。はげしい運動ではなく散歩やストレッチをお勧めします。散歩は1日8000歩を目安にできるとよいと思いますが、自分の体調に合わせて計画してください。ストレッチは姿勢の維持に役立ちます。前かがみや斜め横になる姿勢が起こりやすくなります。自分ではまっすぐと感じる姿勢が、実際には斜めになっていることが少なくありませんので、できるだけ鏡を見て姿勢を良くしましょう。自分では大丈夫と思っていても転倒が起こりやすいので、躓くようなものは片付け早めに手すりを付けます。小さな楽しみを作って、毎日を工夫して過ごしましょう。
私たちは年を取ると病気が増えます。病気は大変ですが、病気をしても楽しんで若い方に生き方の手本を示しましょう。
10. 次の病名はこの病気の別名又はこの病気に含まれる、あるいは深く関連する病名です。 ただし、これらの病気(病名)であっても医療費助成の対象とならないこともありますので、主治医に相談してください。
該当する病名はありません。
11. この病気に関する資料・関連リンク
神経変性疾患領域の基盤的調査研究班 パーキンソン病の療養の手引き
(https://plaza.umin.ac.jp/neurodegen/wp/wp-content/uploads/2025/10/parkinson_tebiki.pdf)
パーキンソン病治療ガイドライン2018
(https://neurology-jp.org/guidelinem/parkinson_2018.html)
治験を実施している指定難病を調べることができます。キーワード検索欄に指定難病名を入力し、検索してください。
治験・臨床研究情報検索サイト一覧