特発性拡張型心筋症(指定難病57)
○ 概要
1. 概要
左室収縮低下と左室内腔の拡張を特徴とする疾患群であり、高血圧性、弁膜性、虚血性心疾患など原因の明らかな疾患を除外する必要がある。
2. 原因
家族性の拡張型心筋症は、外国での報告は20~30%にみられ、平成11年の厚生省の特発性心筋症調査研究班で施行した全国調査では5%である。遺伝子の異常で拡張型心筋症様病態を発症することがあると報告されている。
3. 症状
左心不全による低心拍出状態と肺うっ血や不整脈による症状を特徴とし、病期が進行すると両心不全による臨床症状をきたす。
自覚症状は労作時呼吸困難、動悸や易疲労感の訴えで始まり、進行すると安静時呼吸困難、発作性夜間呼吸困難、起座呼吸を呈するようになる。また、不整脈による脈の欠滞や動悸、あるいは胸部圧迫感や胸痛などをきたすこともある。
心拡大と心不全徴候(頻脈、脈圧狭小、皮膚の蒼白、頸静脈の怒張、浮腫、肝腫大、肝拍動、腹水など)がみられる。
4. 治療法
心移植以外に根治的療法はない。身体活動の調整が必要で、うっ血や低心拍出の症状があるときはできるだけ安静にさせる。食塩制限(5~8g)と水分制限が必要である。左室収縮機能障害に対しては、アンジオテンシン変換酵素(ACE)阻害薬、β遮断薬、サクビトリルバルサルタン、SGLT阻害薬、HCNチャネル遮断薬を用いる。うっ血症状があれば利尿薬を併用する。スピロノラクトンは利尿薬としての作用だけではなく長期予後改善効果が認められている。
重症の心室性不整脈による突然死に対する対策が重要である。β遮断薬は突然死を低下させることが示されている。重症心室性不整脈が出現する場合には副作用に注意しながらクラスⅢの抗不整脈薬アミオダロンの投与を行う。薬物抵抗性の場合には植込型除細動器の使用を考慮する。高度の房室ブロックや洞不全症候群などの除脈性不整脈を合併している場合には恒久的ペースメーカー植え込み術の適応を検討する。
本症では左室拡大を伴うびまん性左室壁運動低下が存在し、左室壁在血栓が生じる場合がある。また、左房拡大を伴う心房細動の例で心房内血栓が生じることもある。その場合、抗凝固療法を行う。
5.予後
前述の厚生省の調査では、本症の5年生存率は76%であり死因の多くは心不全または不整脈である。
男性、年齢の増加、家族歴、NYHAⅢ度の心不全、心胸比60%以上、左室内径の拡大、左室駆出率の低下の存在は予後の悪化と関連する。
○ 要件の判定に必要な事項
1.患者数(令和元年度医療受給者証保持者数)
19,423人
2.発病の機構
不明(一部は遺伝子異常との関連が示唆されている。)
3.効果的な治療方法
未確立(根治療法はない)
4.長期の療養
必要
5.診断基準
あり(現行の特定疾患治療研究事業の診断基準を研究班にて改訂)
6.重症度分類
拡張型心筋症の重症度分類を用いて中等症以上を対象とする。
○ 情報提供元
「特発性心筋症に関する調査研究」
研究代表者 九州大学大学院医学研究院 循環器内科学 教授 筒井裕之
<診断基準>
1 主要項目
基本病態:拡張型心筋症は特発性心筋症※1の中で、左室駆出率低下と左室内腔拡大を特徴とする疾患群であり、多くの場合進行性である。
(1) 自覚症状
呼吸困難、動悸、易疲労感、胸部圧迫感(胸痛)
(2) 他覚所見
頸静脈怒張、肝腫大、肝頸静脈逆流、下腿浮腫、腹水、脈圧狭小
(3) 聴診
Ⅲ音、Ⅳ音、II音肺動脈成分の亢進
(4) 胸部X線
心陰影の拡大、肺うっ血
(5) 心電図
心室性不整脈、心房細動、QRS幅の延長、左房負荷、異常Q波、ST-T異常、左室側高電位、肢誘導低電位、
(6) 心エコー図
左室内腔拡大と駆出率低下(びまん性)
(7) 冠動脈造影※2
びまん性の左室収縮低下の原因となる冠動脈病変を認めない。
(8) 心筋シンチ
心筋灌流低下を高頻度に認める。
(9) MRI
左室内腔拡大と駆出率低下(びまん性)を認める。
(10) 運動耐容能
最大酸素摂取量及び嫌気性代謝閾値(AT)の低下を認める。
(11) 心内膜下心筋生検※2
特異的な組織所見はないが、 種々の変性像や高度の線維化を認める。
(12) 家族歴
家族歴が認められることがある。
(参考)遺伝子解析・その他
ミトコンドリアDNA、心筋β-ミオシン重鎖遺伝子、ジストロフィン遺伝子などの異常によって、拡張型心筋症の病態を示すことがある。
※1 特発性心筋症:昭和58年「厚生省特定疾患特発性心筋症調査研究班」の定義による。
※2 新規申請にあたっては、冠動脈造影は原則として必須である。また、心内膜下心筋生検は、心筋炎や特
定心筋疾患との鑑別のため施行されることが望ましい。
2 除外診断
特発性心筋症とは、原因不明の心筋疾患をいう。高血圧性、弁膜性、虚血性及び以下の疾患は特定心筋疾患specific heart muscle diseaseとして別に扱う。
①アルコール性心疾患、産褥心、原発性心内膜線維弾性症
②心筋炎(原因の明らかなもの、不明のものを含む)
③神経・筋疾患に伴う心筋疾患
④結合組織病に伴う心筋疾患
⑤栄養性心疾患(脚気心など)
⑥代謝性疾患に伴う心筋疾患(Fabry病、ヘモクロマトーシス、Pompe病、Hurler症候群、Hunter 症候群など)
⑦不整脈による心筋症(頻脈及び徐脈)
⑧その他(アミロイドーシス、サルコイドーシス、薬剤性など)
3.診断基準
特発性心筋症において、左室収縮低下及び左室内腔拡大を認め、除外すべき疾患を全て除外したもの
<重症度分類>
中等症以上を対象とする。
拡張型心筋症 重症度分類 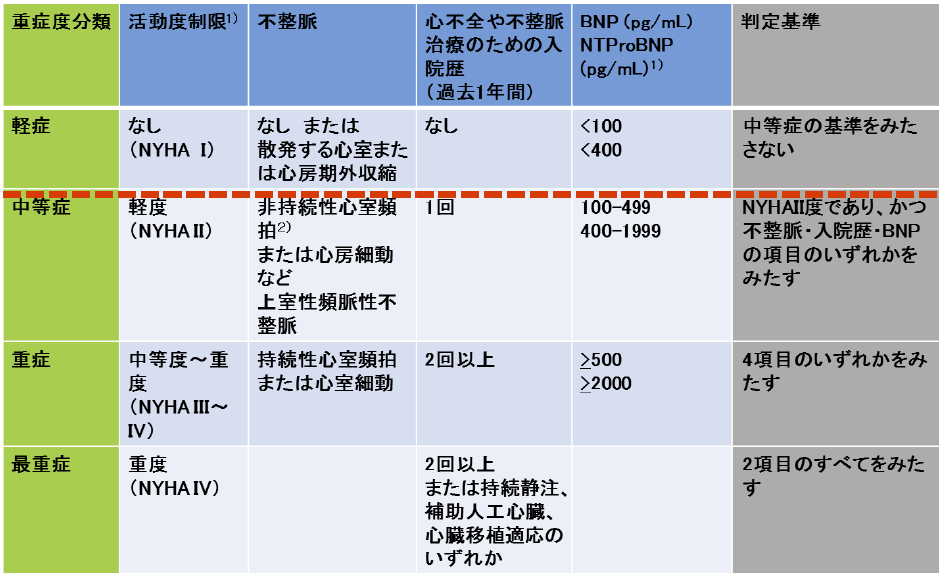
注釈
1)活動度制限とBNP値の判定は患者の状態が安定しているときに行う
2)非持続性心室頻拍:3連発以上で持続が30秒未満のもの
3)補助人工心臓装着中の患者は自覚症状は改善している場合もあるが、重症度としては重症と判定することが妥当と考えられる
4)心臓移植後の患者は自覚症状にかかわらず重症度は重症と判定することが妥当と考えられる
<参考資料>
1)活動度制限の評価に用いる指標
NYHA分類
|
Ⅰ度 |
心疾患はあるが身体活動に制限はない。 |
|
Ⅱ度 |
軽度から中等度の身体活動の制限がある。安静時または軽労作時には無症状。 |
|
Ⅲ度 |
高度の身体活動の制限がある。安静時には無症状。 |
|
Ⅳ度 |
心疾患のためいかなる身体活動も制限される。 |
NYHA: New York Heart Association
|
NYHA分類 |
身体活動能力 |
最大酸素摂取量 |
|
I |
6 METs以上 |
基準値の80%以上 |
|
II |
3.5~5.9 METs |
基準値の60~80% |
|
III |
2~3.4 METs |
基準値の40~60% |
|
IV |
1~1.9 METs以下 |
施行不能あるいは |
NYHA分類に厳密に対応するSASはないが、
「室内歩行2METs、通常歩行3.5METs、ラジオ体操・ストレッチ体操4METs、速歩5-6METs、階段6-7METs」をおおよその目安として分類した。


※診断基準及び重症度分類の適応における留意事項
1.病名診断に用いる臨床症状、検査所見等に関して、診断基準上に特段の規定がない場合には、いずれの時期のものを用いても差し支えない(ただし、当該疾病の経過を示す臨床症状等であって、確認可能なものに限る)。
2.治療開始後における重症度分類については、適切な医学的管理の下で治療が行われている状態で、直近6ヵ月間で最も悪い状態を医師が判断することとする。
3.なお、症状の程度が上記の重症度分類等で一定以上に該当しない者であるが、高額な医療を継続することが必要な者については、医療費助成の対象とする。
- 「心筋症診療ガイドライン(2018年改訂版)」(班長:筒井 裕之、北岡 裕章 掲載:日本循環器学会/日本心不全学会合同ガイドライン)
- 北畠顕, 友池仁暢. 厚生労働省難治性疾患克服事業 特発性心筋症調査研究班. 心筋症, 診断の手引きとその解説. かりん社, 札幌2005
- 心筋症, 診断の手引きとその解説(厚生労働省難治性疾患克服研究事業特発性心筋症調査研究班 北畠顕・友池仁暢 編)
- 松森 昭, 他 特発性心筋症の全国調査. 特発性心筋症調査研究班平成12年度研究報告書 2000, 40-60
- 「心不全診療ガイドライン(2025年改訂版)」(班長:加藤 貴雄 掲載:日本循環器学会/日本心不全学会合同ガイドライン)
- 「2024年改訂版 心臓血管疾患における遺伝学的検査と遺伝カウンセリングに関するガイドライン」(班長:今井 靖 掲載:日本循環器学会/日本心臓病学会/日本小児循環器学会合同ガイドライン)
- 特発性心筋症の診断・ゲノム情報利活用に関する調査研究班ホームページ(https://www.cardiomyopathy.jp/)
- 日本循環器学会ホームページ(https://www.j-circ.or.jp)
- 日本循環器学会専門医名簿(https://www.j-circ.or.jp/senmoni_kensaku/)
- Bozkurt B, Colvin M, Cook J, Cooper LT, Deswal A, Fonarow GC, et al. Current Diagnostic and Treatment Strategies for Specific Dilated Cardiomyopathies: A Scientific Statement From the American Heart Association. Circulation. 2016 Dec 6;134(23):e579-e646. doi: 10.1161/CIR.0000000000000455.
- Zeppenfeld K, Tfelt-Hansen J, de Riva M, Winkel BG, Behr ER, Blom NA, et al. 2022 ESC Guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death. Eur Heart J. 2022 Oct 21;43(40):3997-4126. doi: 10.1093/eurheartj/ehac262.
- Arbelo E, Protonotarios A, Gimeno JR, Arbustini E, Barriales-Villa R, Basso C, et al. 2023 ESC Guidelines for the management of cardiomyopathies. Eur Heart J. 2023 Oct 1;44(37):3503-3626.
- Enzan N, Matsushima S, Ide T, Kaku H, Tohyama T, Funakoshi K, et al. Beta-Blocker Use Is Associated With Prevention of Left Ventricular Remodeling in Recovered Dilated Cardiomyopathy. J Am Heart Assoc. 2021 Jun 15;10(12):e019240.
- Enzan N, Matsushima S, Ide T, Tohyama T, Funakoshi K, Higo T, et al. The use of angiotensin II receptor blocker is associated with greater recovery of cardiac function than angiotensin-converting enzyme inhibitor in dilated cardiomyopathy. ESC Heart Fail. 2022 Apr;9(2):1175-1185.
- Tsutsui Y, Matsushima S, Enzan N, Noda E, Shinohara K, Hashimoto T, et al. Nationwide Temporal Trends in Clinical Characteristics and Treatment of Dilated Cardiomyopathy From 2003 to 2013 in Japan- A Report From Clinical Personal Records. Circ J. 2023 Mar 24;87(4):500-507.
治験を実施している指定難病を調べることができます。キーワード検索欄に指定難病名を入力し、検索してください。
(公財)難病医学研究財団
- 拡張型心筋症に対するヒトiPS細胞由来心血管系細胞多層体(IHJ-301)の治験
治験・臨床研究情報検索サイト一覧